Склероз гиппокампа — это патология, характеризующаяся дегенерацией нейронов в области гиппокампа, который играет ключевую роль в процессах памяти и обучения. Это состояние часто ассоциируется с такими заболеваниями, как эпилепсия, болезнь Альцгеймера и другие неврологические расстройства.
Изменения, происходящие в гиппокампе, могут привести к нарушению когнитивных функций, что затрудняет запоминание новой информации и воспроизведение старых воспоминаний. Понимание механизмов склероза гиппокампа важно для разработки эффективных методов лечения и реабилитации пациентов с нарушениями памяти.
Симптоматическая височная эпилепсия
Кирилловских О. Н., невролог-эпилептолог, к. м. н.
Симптоматическая височная эпилепсия представляет собой разновидность эпилепсии, при которой источник эпилептифорной активности располагается в височной доле головного мозга. Чаще всего ее возникновение связывают со склерозированием медиальных структур височной доли, таких как гиппокамп и рог Аммона. Это состояние получило название мезиальной височной эпилепсии и является наиболее распространенной формой заболевания как у детей, так и у взрослых, составляя 25% среди всех видов эпилепсии и 60% среди симптоматических форм, где припадки являются следствием других заболеваний.
Мезиальная височная эпилепсия проявляется с тремя основными пиками в возрасте 6, 15 и реже 27 лет. Причины развития данного типа эпилепсии остаются не вполне выясненными.
У 15-30% пациентов наблюдались фебрильные припадки, то есть судороги, напоминающие эпилептические, возникающие на фоне высокой температуры у детей. Случаи склероза гиппокампа, зафиксированные на МРТ, в 78% наблюдений были связаны с атипичными фебрильными судорогами.
Фебрильные судороги чаще всего возникают у детей младше 6 лет, после чего следует период, длительность которого составляет от 2 до 7 лет, когда эпилептические припадки отсутствуют, однако могут наблюдаться расстройства интеллекта и поведения. Этот «светлый промежуток» заканчивается появлением афебрильных эпилептических приступов.
Начало мезиальной височной эпилепсии может быть незаметным, например, когда оно стартует с изолированной ауры. Наиболее характерные для этой ауры ощущения – вегетативно-висцеральные.
Приступы могут вначале протекать с сохраненным сознанием, затем приводя к его временной потере. Ауры также могут сопровождаться нарушениями психических функций, такими как дереализация и деперсонализация.
С прогрессированием заболевания изолированные ауры трансформируются в сложные парциальные приступы, способные завершаться генерализованными судорогами. Установить диагноз мезиальной височной эпилепсии затруднительно, так как на ЭЭГ не наблюдается специфических изменений.
Лечение данного типа эпилепсии требует назначения высоких доз противоэпилептических препаратов, которые могут создавать устойчивость к терапии. Эффективность медикаментозного лечения невелика, полный контроль над приступами удается достичь лишь у 25-42% пациентов.
Помимо медикаментозной терапии, используются и другие методы, такие как нейрохирургическое вмешательство. Хирургические методы включают переднюю височную лобэктомию и селективную амигдалогиппокампэктомию, которые рекомендуются пациентам с резистентной формой болезни.
Среди немедикаментозных подходов также имеется VNS-терапия — неинвазивный метод, продемонстрировавший эффективность в случаях тяжелых резистентных форм эпилепсии.
Симптоматическая височная эпилепсия
В наше время симптоматическая височная эпилепсия не следует считать исключительно неблагоприятным состоянием, приводящим к инвалидности. Адекватная фармакотерапия и различные виды немедикаментозного лечения позволяют большинству пациентов достичь ремиссии эпилептических приступов и заметного улучшения качества их жизни.
Причины и симптомы склероза гиппокампа

Мезиальная височная эпилепсия проявляется фокальными приступами с автоматизмами. Основные факторы, способствующие развитию этой патологии, включают:
- значительная утрата нейронов;
- замещение поврежденных участков глиальной тканью, которая изолирует электрические импульсы;
- формирование очагов повышенной возбудимости в оставшихся нервных клетках.
Существуют разногласия по поводу первопричины — является ли мезиально-височный склероз следствием эпилепсии височной доли или наоборот. У 1% детей с впервые установленной эпилепсией изменения в гиппокампе выявляются на МРТ. У взрослых такой склероз фиксируется в 3-10% случаев с двусторонними изменениями, хотя клинические проявления могут быть односторонними.
К причинам атрофии гиппокампа могут относиться:
- черепно-мозговая травма;
- нейроинфекции, такие как герпес, ВИЧ, сифилис и прочие;
- многократные фебрильные судорожные эпизоды;
- определенные заболевания центральной нервной системы;
- генетическая предрасположенность — мутации в генах SCN1A, SCN1B, SCN2A;
- злокачественная астроцитома;
- врожденные аномалии гиппокампа.
Все вышеперечисленные состояния приводят к склерозу в гиппокампе и затрагивают соседние структуры. Заболевание, как правило, проявляется в конце первого десятилетия или в середине второго. У 90% пациентов первый приступ фиксируется до 16 лет, с пиковыми возрастными периодами в 6, 15 и 27 лет.
Признаки склероза гиппокампа на МРТ
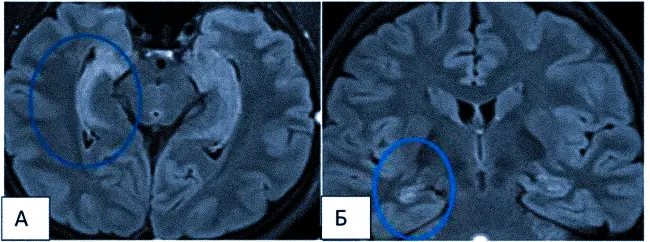
Метод магнитно-резонансной томографии является основным для оценки состояния гиппокампа. Признаки, указывающие на склероз гиппокампа на МРТ, включают:
- уменьшение объема гиппокампальной структуры, атрофические изменения соседних участков головного мозга;
- вторичное расширение височного рога бокового желудочка и хориоидальной щели;
- размытость границ между серым и белым веществами;
- аномальная форма гиппокампа;
- асимметричное развитие гиппокампов;
- нечеткость интравентрикулярной части аммонова рога;
- атрофия свода головного мозга со стороны поражения;
- гиперинтенсивные очаги в гиппокампе на изображениях в режимах T2 и FLAIR.
Фармакорезистентная эпилепсия
Эпилепсия — это заболевание головного мозга, проявляющееся повторяющимися приступами, вызванными аномально активными нейронными разрядами (эпилептическими приступами) и сопровождающееся разнообразными клиническими и параклиническими симптомами. Одиночный эпилептический приступ не считается заболеванием.

- наличие как минимум двух неспровоцированных (или рефлекторных) приступов с интервалом более 24 часов;
- наличие одного неспровоцированного (или рефлекторного) приступа, с высокой вероятностью повторения, аналогичной риску рецидива после двух спонтанных эпизодов в течение следующих 10 лет;
- наличие эпилептического синдрома.

Рис. 1. Структура классификации эпилепсий по данным Международной противоэпилептической лиги (2017 г.)

Рис. 2. Расширенная рабочая классификация типов эпилептических приступов по данным Международной противоэпилептической лиги (2017 г.)
Эпилепсия является полиэтиологичным заболеванием. Все ее формы классифицируются по причинам на 6 категорий:
Структурные
- Структурные формы включают различные виды повреждений;
Фармакорезистентная эпилепсия: причины, диагностика и методы лечения
- церебральные дизонтогенезы, или нарушения развития коры — одна из самых частых причин эпилепсии у детей и подростков; часто вовлекаются обе гемисферы (например, лисэнцефалия) или наблюдаются двусторонние повреждения (билатеральная узловая гетеротопия), либо поражение одной гемисферы целиком (гемимегалэнцефалия), либо изолированные участки в коре одного полушария (фокальные кортикальные дисгенезии);
- фокальная кортикальная дисплазия (ФКД) — это участок мальформации коры, варьирующий по величине и расположению. Локальные изменения могут выражаться в аномалиях клеток (цитомегалия нейронов, баллонные клетки), неправильном расположении нейронов в слоях неокортекса или в подкорковом белом веществе, дезорганизации коры и полимикрогирии. ФКД часто сопровождается интериктальной эпилептиформной активностью на ЭЭГ, а приступы могут проявляться в любом возрасте и часто резистентны к лекарственной терапии.

Рис. 3. МР-томограмма пациента с фокальной кортикальной дисплазией правой лобной доли
- склероз гиппокампа — наиболее распространенное структурное изменение мозга у пациентов с фармакорезистентной эпилепсией; характеризуется уменьшением объема гиппокампа, повышением сигнала на T2-взвешенных изображениях и нарушением внутренней структуры. Операции на височной доле у таких пациентов в 2/3 случаев приводят к исчезновению приступов с потерей сознания.

Рис. 4. МР-томограмма пациента с левосторонним склерозом гиппокампа (коронарные и аксиальные срезы).
- Формирование дефектов в головном мозге может вызывать появление судорог, если они приводят к сжатию или вовлечению корковой области мозга в патологический процесс. Примерами таких аномалий являются менингиомы и растущие глиомы с диффузным инфильтративным характером. В отдельную категорию выделяются доброкачественные новообразования, которые связаны с длительной фармакорезистентной эпилепсией (опухоли, ассоциированные с долговременной эпилепсией, LEATs).

Рис. 5. МР-томограмма пациента с глионейрональной опухолью в средних областях левой височной доли

Рис. 6. МР-томограмма пациента с кавернозной ангиомой левой лобной доли
- Травмы головного мозга являются основной причиной развития приобретенной структурной эпилепсии. Судороги, которые возникают в течение первых суток после травмы, обозначаются как немедленные; а те, что появляются через неделю и позже, считаются поздними. В большинстве случаев, более 90%, посттравматическая эпилепсия развивается в течение первых двух лет после травмы.

Рис. 8. Компьютерная томография и 3D-реконструкция пациента с установленными инвазивными электродами.
Генерализованная эпилепсия не связана с конкретным участком мозга, который бы отвечал за возникновение судорог. Предполагается, что это заболевание имеет генетическую природу.

Рис. 9. Разновидности приступов и соответствующие параметры на ЭЭГ
- резекционные вмешательства, с удалением очага, вызывающего эпилепсию;
- операции со стимуляторами, в ходе которых имплантируют устройство, передающее электрические сигналы в участки нервной системы;
- интерстициальная лазерная термотерапия.

Рис. 10. Различные виды хирургических операций при эпилепсии

Рис. 11. МР-томограмма пациента с правосторонним склерозом гиппокампа до операции

Рис. 12. КТ-томограмма пациента после хирургического вмешательства (амигдалогиппокампэктомия справа)
Стимуляционные методы терапии применяются для лечения форм эпилепсии, стойких к лекарственным средствам. К ним относятся глубокая стимуляция мозга (Deep Brain Stimulation, DBS) и стимуляция блуждающего нерва (Vagus Nerve Stimulation, VNS).

Рис. 13. Схема VNS-терапии в хирургическом лечении эпилепсии

Рис. 14. Схема DBS-стимуляции в хирургическом лечении эпилепсии
- уделить внимание сбору анамнеза;
- провести анализ дневника наблюдений за приступами;
- заснять на видео приступы для последующей оценки;
- изучить неврологический статус пациента;
- провести анализ данных видеомониторинга ЭЭГ.
Фармакорезистентная эпилепсия
- долгосрочный видео-ЭЭГ-мониторинг (ночной, суточный и многодневный); продолжительность исследования устанавливается эпилептологом после тщательного опроса;
- провести МРТ головного мозга (рекомендуется взять с собой снимки на диске; при необходимости врач может назначить МРТ с более высоким разрешением, следуя протоколу эпилепсии);
- произвести нейропсихологическую оценку состояния пациента (особенно актуально при выборе метода стимуляции).

Рис. 15. Схема подходов к лечению пациентов с фармакорезистентной эпилепсией
Нейровизуализация и магнитно-резонансная томография (МРТ)
Уровень диагностики МВС значительно улучшился благодаря прогрессу в нейровизуализации, особенно используя МРТ. Этот метод является предпочтительным для обнаружения структурных изменений в височной области мозга. Ключевые аспекты МВС на МРТ могут включать:
- Атрофия гиппокампа: это наиболее выделяющийся признак, проявляющийся в уменьшении объема гиппокампа. Атрофия может быть односторонней или двусторонней и связана с уровнем тяжести симптомов.
- Гиперинтенсивность на T2 и FLAIR: увеличение сигнала в гиппокампе, сигнализирующее о наличии глиоза или иных дегенеративных изменений.
- Утрата нормального стратифицированного рисунка гиппокампа: в норме гиппокамп демонстрирует четкое слоистое строение, которое может быть нарушено.
- Асимметрия височных рогов боковых желудочков: расширение височного рога на больной стороне ввиду атрофии соседних структур.
- Аномальные сигналы в зубчатой фасции: такие изменения могут быть показателями ранней стадии дегенерации, предшествующей полной атрофии гиппокампа.
Использование этих признаков на МРТ имеет критически важное значение для ранней диагностики и точного определения местоположения эпилептогенного очага.
Клинические проявления LATE-энцефалопатии
Основной симптом LATE-энцефалопатии — это нарушение эпизодической памяти у пациентов старше 80 лет. Этот признак сближает LATE-энцефалопатию с болезнью Альцгеймера, и дифференциация между ними представляет собой сложную задачу. В клинической практике LATE-энцефалопатия сопровождается преимущественным нарушением памяти, не затрагивая при этом настроение и поведение. В отличие от болезни Альцгеймера, при LATE-энцефалопатии также отсутствует афазия и психотические проявления. Таким образом, течение LATE-энцефалопатии можно считать более благоприятным, хотя применение термина «доброкачественный» к прогрессирующему неврологическому заболеванию, которое приводит к утрате самостоятельности, является спорным.
Явные различия можно наблюдать и между LATE-энцефалопатией и лобно-височной деменцией, связанной с отложением TDP-43 в нейронах. LATE-энцефалопатия проявляется у пациентов старше 80 лет, тогда как лобно-височная деменция может развиваться у людей моложе 50 лет.
Лобно-височная деменция сопровождается эмоциональными изменениями, включая уплощение эмоций, их грубость и стереотипность. Также может наблюдаться нарушение социального дистанцирования или проявление сексуальной расторможенности. В отличие от этого, LATE-энцефалопатия не сопровождается такими симптомами, а ведет к деменции с преобладанием нарушений памяти.
Нейровизуализация у пациентов с LATE-энцефалопатией показывает изменения в лимбической системе мозга, что не характерно для лобно-височной деменции. Лобно-височная деменция, в свою очередь, вызывает более значительные и выраженные изменения в коре головного мозга по сравнению с LATE-энцефалопатией.
Что приносит новый тип деменции?
Исследователи подчеркивают, что выделение LATE-энцефалопатии как отдельного заболевания — это только начало. Ожидается еще много исследований, которые помогут прояснить причины и течение этого состояния, а также разрабатывать подходы к лечению. Однако признание LATE-энцефалопатии уже дало положительные результаты.
В настоящее время в клинических испытаниях наблюдается множество пациентов пожилого возраста, которые демонстрируют снижение когнитивных функций с преобладанием нарушений памяти и атрофией гиппокампа, но при этом у них не выявляют характерный для болезни Альцгеймера амилоидоз. Доля таких пациентов может достигать 15-30% от общего числа участников исследования. Каковы их диагнозы? С чем они сталкиваются? LATE-энцефалопатия является ответом на эти вопросы.
Некоторые случаи деменции, ошибочно рассматриваемые как проявления заболевания Альцгеймера, могут на самом деле быть вызваны нейродегенеративным процессом, описанным в отчетах. Это относится и к пациентам старше 80 лет — учитывая рост этой возрастной категории благодаря достижениям медицины. К сожалению, не существует надежных биомаркеров LATE-энцефалопатии, за исключением обнаружения отложений TDP-43 в нейронах и глиальных клетках. Мы не можем проводить биопсии головного мозга у всех пациентов, у которых есть подозрения на LATE-энцефалопатию. Таким образом, требуется разработать более безопасные методы, нежели инвазивные вмешательства.
Одно из возможных решений заключается во внедрении системы ATN, которая помогает отличать случаи деменции при болезни Альцгеймера от других типов деменции с «альцгеймеровскими» симптомами. С использованием различных методов нейровизуализации мы можем определить, имеются ли у пациента бета-амилоид и тау-протеины, а также идет ли в головном мозге процесс нейродегенерации.
Случаи, когда проявляются клинические симптомы деменции Альцгеймера, но структурные и молекулярные изменения не соответствуют этому диагнозу, формируют группу SNAP (подозреваемая непатология Альцгеймера). Это деменции с патогенезом, отличным от болезни Альцгеймера. Различия в патогенезе требуют различного подхода к лечению заболеваний.
К сожалению, амилоидная гипотеза болезни Альцгеймера подвергается серьезным критическим замечаниям: препараты, направленные на устранение бета-амилоида или предотвращение его накопления, не демонстрируют ожидаемых результатов в клинических испытаниях. Основная причина, обсуждаемая специалистами, состоит в том, что отложение бета-амилоида — это не причина болезни Альцгеймера, а сопутствующий процесс.
На данный момент мы не выявили ключевой механизм патогенеза, что лишает нас возможности вмешаться в данный процесс. Упомянутая LATE-энцефалопатия предоставляет второе, альтернативное объяснение вопроса о неэффективности амилоидснижающих препаратов при болезни Альцгеймера. Эта альтернатива гласит, что у определенной категории пациентов может быть не болезнь Альцгеймера, а именно LATE-энцефалопатия. Если это подтвердится, нам будет необходимо разрабатывать новые подходы к лечению, отличные от существующих методов терапии деменции.